
Prof. Dr. SÜLEYMAN L. DİNÇER
HEMATOLOJİ UZMANLIK DERNEĞİ YÖNETİM KURULU BAŞKANI
TARİHÇE
Hiroşima ve Nagazaki’de radyasyona maruz kalan hastalarda görülen hematolojik etkiler, kemik iliği nakli ve kök hücre hakkındaki araştırmaları stimüle etmiştir. 1950’ler ve 1960’lar boyunca bilim adamları, kanın yeniden yapılması kemik iliği hücrelerinin damar yolu ile verilmesi yoluyla tamamıyla yeniden oluşturabileceklerini bulmuştu. Hematoloji uzmanları doktorlar, hem kalıtsal ve sonradan kazanılmış kemik iliği yetmezliği sendromlarını ve gelişmiş olan malign (kanser) hastalığı tedavi etmek için kullanılan kemoterapinin (ilaçla tedavi) ve yüksek doz radyasyonun (ışın) ölümle sonuçlanabilme ihtimali olan iliği yok edici etkilerinden hastaları kurtarmak için; kemik iliği naklinin (elde edilen kök hücelerin) (Resim 1) yararlarını gördüler.
Kök hücre ; kemik iliği oluşturan elemanları yok olmuş bir alıcının tüm hematopoetik ve lenfoid sistemini yeniden oluşturma kapasitesine sahip bir hücre olarak tanımlanabilir. Başlangıçtaki ilk denemeler, otolog yani kendisinden elde edilen naklin tersi olarak allojenik (HLA sı uygun kardeşi ve bir başkasından) nakil ile gerçekleşmiştir. Allojenik transplantasyondaki en önemli sorun; hem donörün iliğinin alıcı tarafından reddinde hem de alıcının dokularına karşı donörün immünolojik olarak olgun lenfositleri tarafından geliştirilen reaksiyon olan graft versus host hastalığının (GVHD vericinin alıcı hastaya saldırısı) oluşturduğu atılım (rejeksiyon) reaksiyonuydu. 1960’ların ortalarında HLA (Human Lokosit Antijeni) sisteminin bulunması, klinisyenlere kardeş donör/alıcı çiftleri arasında birbirini tutan kardeşinden başarılı nakil yapmalarını sağladı. Uygun dozda radyasyon iliği yok edici kemoterapotik ilaçlar ve rejeksiyonu önlenmesi için kullanılan ilaç tedavilerin saptanmasına yönelik araştırmaların memnun edici sonuçları ile bu yöntemin başarısı kanıtlandı. 1970’lerin sonuna kadar, allojenik (kardeşinden) nakil, büyük ölçüde deneysel ve genellikle ölümcül sonuçlanan aplastik aneminin, immün (vücut savunma sistemi ) yetmezlik sendromlarının ve birçok lösemi çeşidinin iyileştirilebildiğine dair bulguların objektif olarak belirlenmesi sonucu kabul gören bir tedavi yöntemi haline geldi.
Kemik iliği nakli uygulama şekilleri
Kök hücre ; kemik iliği oluşturan elemanları yok olmuş bir alıcının tüm hematopoetik ve lenfoid sistemini yeniden oluşturma kapasitesine sahip bir hücre olarak tanımlandığına göre, teorik olarak bu sadece bir kök hücreyle başarılabilir, ancak klinik uygulamada alıcının vücut ağırlığına göre kilo başına en az 1-3 X 108 nukleuslu kemik iliği hücresinin infüzyonu, kalıcı ve hızlı iliğin tutmasını sağlamaktadır. Bunlar morfolojik olarak lenfositlerden ayırt edilemez, ama CD34+ gibi karakteristik bir hücre yüzey antijen yapısına sahiptir.
Kök hücre kaynakları
Transplantasyon için kemik iliği kök hücreleri, kalça kemiğinden, ilik kavitesine kemik iliği için özel iğnelerin sokulması ve alınması yolu ile elde edilir. Bu prosedür genellikle ameliyathane şartlarında genel anestezi altında yapılır. Alıcının ağırlığına göre kilogram başına 15-20 mL’lik bir sıvı kemik iliği toplanır ve bir işleme tabi tutmadan veya bunu alıcıya vermeden etmeden önce kemik parçaları ile diğer hücre kümelerini ayırmak için filtre edilir. Kemikten İlik alma işi genellikle iyi tolere edilir. Ancak donöre ait riskler azda olsa vardır. Genel anestezinin riskleri ve de çok nadiren bu bölgeden olan abondan bir kanama veya yanlış yere uygulanmış aspirasyon iğnelere bağlı nöronal hasar ile sınırlı olarak kabul edilebilir.
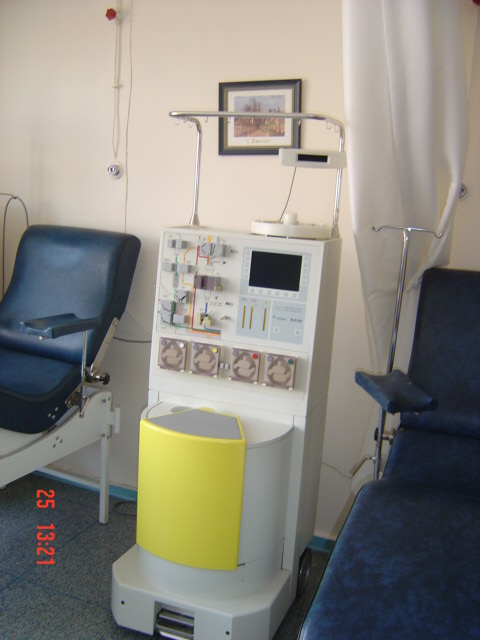
1981 yılında Körbling ve arkadaşları, kök hücelerin alternatif kaynağı olarak çevre kanı kök hücre kullanımını tanımlamış ve klinik uygulaması gerçekleştirilmiştir. Malign bir hastalığa sahip olan şahıslarda yüksek doz kemoterapiden sonra ya da tek başına uyarıcı ilaçlarla; çok sayıda kök hücrenin kemik iliği ortamından ayrılarak periferik kana katıldıkları ve bir ya da daha çok aferez (Resim 2) işlemi ile kolaylıkla toplanabildikleri bilinmektedir. Stimule edilerek kök hücrelerin çıkartıldığı yer olarak çevre kanı, neredeyse tamamiyle otolog transplantasyon için bir hücre kaynağı olarak ilik ile yer değiştirir . Bu işlemin avantajları, kolay toplama, nakilden sonra çok daha hızlı kök hücrenin tutması ve potansiyel olarak daha az tümör bulaşmasıdır.
Üçüncü kaynak: Göbek kordon kanı
Üçüncü bir potansiyel kök hücre kaynağı ise 1988 yılında Gluckman ve arkadaşları tarafından ilikten çok daha fazla konsantre ön hücre içerdiği görülen göbek kordon kanının olduğunu bildirmiştir. Doğum esnasında anneye veya yeni doğana zarar vermeksizin 250 mL’ye kadar toplanabilir. Anrelated (akraba olmayan) allojenik transplantasyon konusunda, kordon kan bankası ile yeni bir devrim başlatılabilir umudu taşımakla birlikte kordon kanı yetişkin alıcılara güvenilir şekilde engraft etmek üzere yeterli miktarda kök hücreler içermeyebilir . Bunlarla birlikte son birkaç yılda ayrıca fetal kemik kavitesinden elde edilebilecek ön hücrelerden de belki de daha az ve doku uyumu aranmadan kemik iliği nakli veya organ naklinin oluşabileceğine dair bazı kanıtlar elde edilmiş ve çalışmalar birçok laboratuvarda yarışırcasına devam etmektedir.
Gerçek transplantasyon prosedürü, toplanan kök hücre konsantresinin intravenöz yolla verilmesidir. Kök hücreler, tam olarak anlaşılamamış olan mekanizmalar ile kemik iliği kavitesine kolayca yerleşmektedir, ve ilk nötrofillerin tutması için geçen 10 ila 25 günün ardından trombositler ve eritrositler de tutar. Bu, donör kök hücrelerinin tutmasını gösterir. Bu bilgiler ışığında kemik iliği nakli kısaca ikiye ayrılır.
Kardeşinden nakil (Allojenik transplantasyon)
Kardeşinden nakil, artan sayıda sonradan olma ve genetik hastalıklar için bir tedavi seçeneğidir. Tedaviye bağlı yüksek mortaliteden dolayı, öncelikli olarak lösemi veya aplastik anemi olmak üzere yaşamı tehdit eden sonradan olma hematolojik hastalıkları olan hastalar üzerinde yapılmış ve yapılmaktadır. Bu prosedürle ilişkili mortalite oranları düştükçe, orak hücreli anemi gibi kronik ancak ölümcül olmayan konjenital hastalıklar için allojenik transplantasyon çok daha fazla olağan ve yapılabilir hale gelmiştir. Malign hastalıklarda otolog transplantasyona kıyasla, allojenik transplantasyonun bilinen birçok potansiyel avantajları vardır. Allojenik transplantasyon, alıcıya normal bir donörden kök hücreleri sağlamakta ve hastalığın tekrarlamasına katkıda bulunabilecek tümör hücrelerinin yeniden verilmesi riskini yok etmekte veya azaltmaktadır. Bazı malign hastalıklarda özellikle başta kronik miyeloid lösemi olmak üzere, bazı malign hastalılarda donör hücreleriyle nakil edilen immünolojik antitümör etkisi bilinmektedir.
Kardeşleri , akraba veya akrabadışı donör (verici) seçimi
Uygun bir allojenik donörün seçimi için majör histokompetibilite kompleksi (MHC) antijenlerinin karşılaştırması (matching), temeli teşkil eder. İnsanlarda bu antijenlere, Human lokosit antijeni (HLA) adı verilir ve vücuttaki tüm çekirdekli hücrelerin hemen hepsinde bulunur. Bu antijenler, immun cevabı oluşturmada önemli işlevleri vardır.
Çoğu allojenik donör, HLA’sı birbirine uyan kardeşlerdir. Birbirine uyan kardeş donörler, HLA tip I A, B ve C’ antijenleri ve de tip II DR, DQ ve DP’ antijenleri benzerdir. Donör ve alıcı tek yumurta ikizi olduğu takdirde singeneik transplantasyonun denir ki hiçbir doku reddi veya GVHD riski yoktur.
Diğer türlü, allojenik transplant için elverişli hastaların yalnızca %25-30’u, HLA’sı uyan bir kardeşe sahiptir. Birbirine uygun bir kardeşi olmayan hastalar için, kısmen uyumlu bir ebeveynden, diğer akrabalardan veya HLA’sı uymuş Unrelated (akraba olmayan) bir donörden transplantasyon düşünülebilir ve GVHD ve diğer posttransplantasyon komplikasyonlarının potansiyel yararları ve artan riskleri var olduğu bilinmektedir. Unrelated kemik iliği naklinden sonra veya kısmi olarak birbirini tutan transplantasyonlardan sonra uzun dönemli hayatta kalma oranı, özellikle yetişkin hastalarda graft rejeksiyonu, enfeksiyon ve GVHD’nin daha yüksek oranlarda gelişmesi ile HLA uyumlu kardeş transplantasyon sonuçlara göre iyi değildir.
Nakil öncesi hazırlama
Kardeşinden transplantasyon için bir endikasyon ortaya konulup uygun bir donör tespit edildikten sonra, hastanın nakil öncesi hazırlama süreci başlar. Hazırlamanın şekli, altında yatan ve tedavi edilecek hastalığa bağlıdır. Ancak, altında yatan hastalıktan bağımsız olarak, hazırlama rejimini kemik ilkiği sorumlu hekimi belirlenen standartlar çerçevesined son şeklini verir.
Dönörden kök hücre temini ve transplantasyon
Yeterli sayıda kök hücrenin temini, başarılı ve sürekli engrfatment için gereklidir. Kemik iliği naklini yapan ekipin belirlediği yöntemle kök hücre toplanır ve nakil için hazırlanır. Çok sayıda CD34 + kök hücreleri olan graftlar da düşük oranda doku reddi ve transplant sonrası enfeksiyöz komplikasyonlar olduğu bildirilmiştir.
Nakil sonrası gelişebilecek sorunlar
En önemli ve en sık rastlanan erken yan etki enfeksiyöz olanlardır. Bir diğer önemli yan etki ise “Graft Versus Host” hastalığıdır. Uygulanan proflaktik önlemlere rağmen, enfeksiyöz komplikasyonlar kök hücre transplantasyonunda başlıca morbidite ve mortalite kaynağıdır. Bunlar bakteriyel, mantar ve viral orjinli olabilir. Ayrıca mide barsak sistemini ilgilendiren ishal, karın ağrısı, kanama ve mukozit yanında karaciğer anormallikleri sıklıkla karşılaşılan sorunlardır. Ayrıca bilinen birçok geç etkileri vardır. Ama hastanın hastalığında daha önemli olmayıp sıklıkla kontrol edilebilir.
Kerdeşten naklin faydası
Kardeşinden nakil sonrası elde edilem fayda altında yatan nakil sebebi diğer hastalığa ve donör ile alıcı özelliklerine bağlıdır. Akut miyelositik lösemi (AML) için nakil, hasta remisyonda iken yapıldığı zaman en etkilisidir. İlk remisyon esnasında gerçekleştirildiğinde, uzun dönemli yaşayabilenlerin yüzde 40 ila 70’inin iyileştirildiği görünmektedir. Tekrar nüksetme zamanında veya sonraki remisyonlar esnasında yapıldığında, bu oranlar artmış nüksetmeden dolayı %20-40’a düşer. Transplant-bağlantılı ölümde, bu geç-safha hastalarda yükselir. Yalnızca kemoterapi ile tedavi edilen AML hastalarının %20-25’inin iyileşebildiği ve konvansiyonel kemoterapiden sonra hastalığı tekrar nüksedenlerin %20-40’ının daha sonra allojenik transplant ile tedavi edilebildiğinden dolayı, transplant zamanlaması sık sık tartışmalıdır ve ilk remisyonda yüksek nüksetme riski altında olan hastaları tespit etme ve bunları derhal transplante etme konusunda fikir birliği vardır.
Kendinden (Otolog) transplantasyon
Hastanın kendisinden önceden toplanmış kök hücrelerin hastalığı yok etmek için yapılacak bir tedavi sonrası hastaya verilme işlemi olarak tanımlayabiliriz. Çoğu kemoterapatik ajanlar ve ışınnın doz sınırlayıcı toksisitesi, kemik iliğinin baskılamasıdır. Bu ajanların çoğunun dozları, eğerönceden toplanarak depolanmış olan kök hücreleri ile önemli ölçüde artırılabilir. Otolog transplantasyonun yararlı olması için, kanser için verilen kemoterapi ve/veya ışına karşı bir doza bağlı cevaba sahip olmalıdır, yani kök hücre tedavisine olanak veren daha yüksek dozlar, tedaviye bağlı morbidite ve mortaliteyi önemli derecede yükseltmeksizin daha fazla tümör hücresini ölüdrebilir ve hatta tamamen yok edebileceği tartşılmaktadır. Otolog transplantasyon, tüm hematopoetik ve immün sistemlerin diğer bir bireyden alınanlarla değiştirilmesini içermediğinden, allojenik transplantasyondan sonra meydana gelen komplikasyonların çoğu –doku reddi, verilen dokunun hastaya karşı reaksiyonu olan GVH hastalığı ve uzatılmış vücut savunma sistemi baskılaması ile ilgili enfeksiyöz komplikasyonlar gibi- bir sorun değildir. Ancak, herhangi bir dokunun hastaya karşı reaksiyonu olan GVH hastalığının olmaması ve tümör hücrelerinin verilen doku ile muhtemel yeniden verilmesi; çoğu kanser veya tümörler için otolog nakillerde daha yüksek bir hastalığın tekrar etmesi ile sonuçlanabilme ihtimalinin iki nedenidir.
Uygun hale getirme ve transplantasyon
İşlemden sonra, doku donmuş haldedir ve hasta kemo/radyoterapinin miyeloblatif dozlarla hazırlama tedavisine girer. İlaç rejimi; tedavi edilen spesifik tümöre karşı ajanların aktivitesine dayanarak seçilir. Aynı zamanda, diğer organ hasarı ile değil ama miyelotoksisite tarafından doz-sınırlayıcı olan bir rejim ayarlamak da önemlidir. Örneğin; sisplatin otolog transplantasyonda nadiren kullanılır çünkü renal toksisite, letal miyelotoksisitenin önünde doz-sınırlayıcıdır. Tedavinin tamamlanmasından ve kemoterapatik ajanların aktif formlarının tüm metabolizmasına ve salgılanmasından sonra önceden toplanmış ve dondurulmuş kök hücre eritilir ve intravenöz olarak yeniden infüze edilir. Takip eden nakil süresi, daha önce tartışılan kardeşinden nakil e başlarlar ve nakilden sonra 6-12 haftaya kadar tam performans durumuna geri dönebilirler. Kardeşinden nakil olan hastaların tersine, otolog transplantasyon hastaları erken doku reaksiyonu (gvhd) ratlanmazken , viral ya da fungal enfeksiyonlar gibi geç komplikasyonları çok daha az yaşarlar. Katarakt, tiroid disfonksiyonu ve infertilite gibi uzun dönemli toksisiteler ışın dan meydana gelebilir ve son çalışmalar, hastaların %10’unun dokusunda uzun yıllar sonra sekonder miyelodisplazi geliştirebileceğini göstermektedir.
Otolog nakilin amaçları spesifik kansere ve klinik duruma bağlı olarak değişir. Akut lösemi ve bazı lenfomalarda, tedavi veya en azından uzun dönemli hastalıktan bağımsız yaşama hastaların önemli bir bölümünde bildirilmiştir. Mültipl miyelomada, bir otolog nakilden sonra tedavi muhtemel görünmemektedir, fakat yapılmış olan çalışmaların sonuçları, otolog nakil , standart kemoterapiden çok daha uzun dönemli hastalıktan bağımsız aralıklar yarattığını göstermektedir. Meme kanserinde otolog nakil IV.evre metastatik meme kanseri için transplante edilen hastalarda neredeyse imkansızdır Ancak meme kanserinde en umut vaat edici uygulama yüksek riskli II veya III.safha hastalıklı hastalarda yoğun bir konsolidasyon tedavisi olarak otolog nakil bir alternatif olabilir.